水蒸气是组成空气的几种气体之一。例如,如果一个系统(如海平面上的空气)的总压力为101.3kPa(或29.9英寸汞柱),而空气由氮气、氧气、水蒸气和其他微量气体组成,这些气体中的每一部分都贡献了101.3k Pa的总压力。水蒸气的部分称为水蒸气分压。水蒸气的分压是定义所有其他湿度参数的公式中的一个关键度量。
压力变化的影响
道尔顿定律:
根据道尔顿定律,气体混合物的总压力等于其组分的分压之和。这意味着组分的份压等于总压力乘以组分摩尔分数的乘积。
因此,气体混合物在不变成分下总压力的变化会导致每个组分的分压变化。例如,气体混合体的总压力增加一倍会导致每个组成部分的分压增加一倍。随着总压力的增加,水蒸气的分压也会相应增加。这是一个需要理解的重要事实,正如你在定义相对湿度和露点温度时所看到的。封闭系统的压力增加会增加相对湿度并提高露点温度,直到达到饱和。
液体上方的蒸汽压力
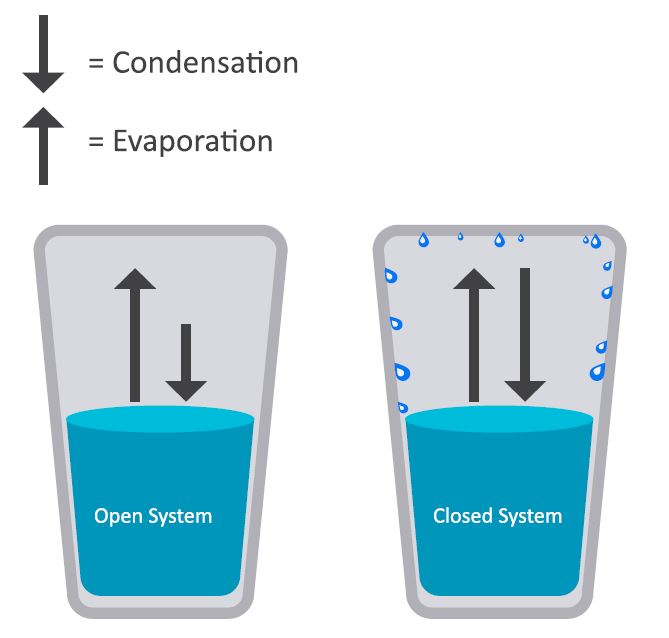
因为液体中的分子比气体中的分子更接近,所以分子间的力比气体中的力更强。液体要汽化,分子间的力必须由分子的动能来克服。如果液体放在密闭容器中,进入气相的颗粒就无法逃逸。在随机运动中,粒子撞击液体并被分子间力重新捕获。因此,两个过程同时发生:蒸发和冷凝。蒸发率随气温升高而增加。这是因为温度的升高对应着分子动能的升高。同时,随着气相中颗粒数量的增加,凝结速率增加:更多的分子撞击液体表面。
当这两个过程相等时,气相中的颗粒数量和压力就稳定了。
平衡蒸汽压力的值取决于液体颗粒之间的吸引力和液体的温度。液体上方的蒸汽压力随着温度的升高而增加。
饱和水蒸气压力
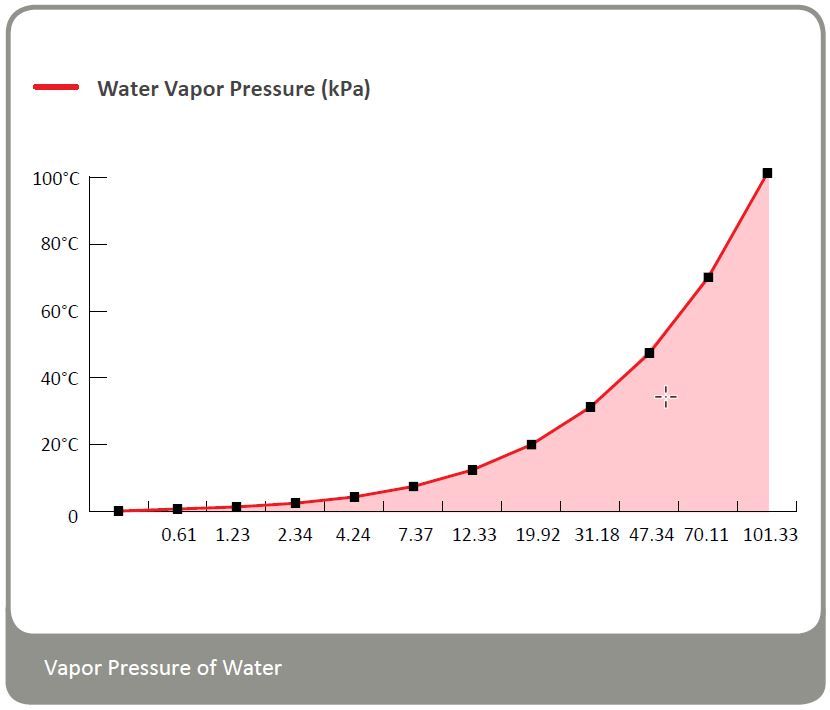
水蒸气压力随着温度的升高而强烈饱和。
冰之上蒸汽压力
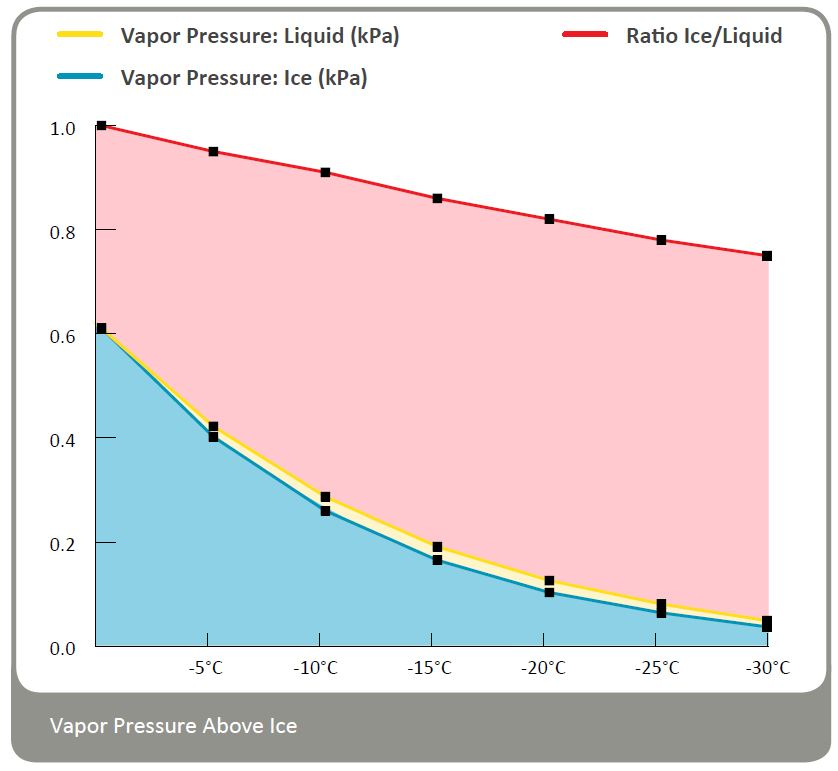
当水结冰时,分子会假设一种允许分子之间进行最大数量氢键相互作用的结构。由于这种结构有大六边形孔,冰比液态水更开放且密度更小。由于冰中的氢键比液态水中更强,分子间的吸引力在冰中最强。这就是为什么冰上的蒸汽压比液态水上的蒸汽压小。